Diagramma di stato dell'acqua:
Tutti i punti delle curve rappresentano situazioni di equilibrio tra i due passaggi di fase opposti, ad es. nel tratto di equilibrio tra liquido-gas, la velocità di evaporazione =alla velocità di condensazione,
nel tratto solido-liquido la velocità di solidificazione=alla velocità di fusione...
Nel diagramma di fase dell'acqua [che notoriamente ha Teb = 100°C e Tcr =°C, alla P di 1 atm (che è la p “ atmosferica”)],
notiamo che nel tratto liquido-gas c'è diretta proporzionalità tra P e T:
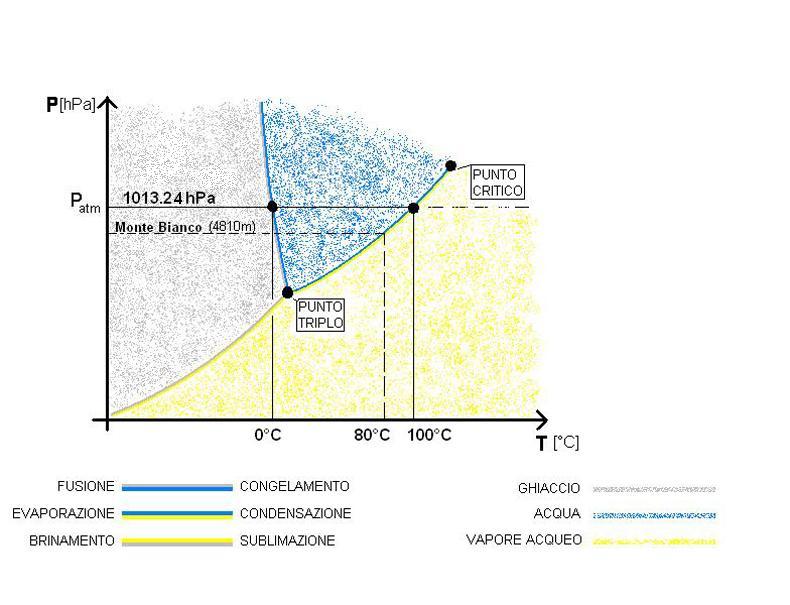
es.supponiamo di stare in montagna, ove la p è < della p atmosferica (1 atm), la Teb sarà < di 100°C => diretta proporzionalità tra P e T.
Mentre, sempre nel diagramma di fase dell'acqua, nel tratto solido-liquido, detto anche “retta delle fusioni”, c'è inversa proporzionalità tra P e T: es.supponiamo sempre di stare in montagna, ove la p è < della p atmosferica (1 atm), la T inizio gelo sarà > di 0°C => inversa proporzionalità tra P e T.
Ora bellissima nonché gettonatissima domanda di orale,
da parte sopattutto di prof. esperti:
confronto tra i diagrammi di stato dell'H2O e della CO2,
proprio a riguardo della diversa pendenza della retta delle fusioni:

Per l'acqua si ha, a livello della retta delle fusioni, una inversa proporzionalità tra P e T, perché per l'acqua ( e per pochissime altre sostanze!), il volume specifico allo stato solido [data la presenza, nel ghiaccio, dei legami a H (vedi! nel file sulle "forze intermolecolari" che ho allegato a fine pagina)] è > del volume specifico allo stato liquido.
Facciamo un esempio:
supponiamo di avere un sistema in equilibrio tra solido e liquido: 50% solido e 50% liquido, cioè stiamo su un punto della retta delle fusioni a una data T e P;
se a un certo punto noi aumentiamo la Pressione esercitata sul sistema, ovvero diminuiamo il volume a disposizione del sistema, il sistema, per il Principio dell'equilibrio mobile di Le Chatelier, per non risentire dell'alterazione apportata, si “sposterà” verso il lato ove “occupa meno spazio”, ovvero verso la fase liquida, fondendo parte del ghiaccio in acqua liquida: in quell'istante non si è più all'equilibrio, ma ad es. sarà 40% solido e 60% liquido;
affinché si ritorni in un “nuovo” stato di equilibrio, deve risolidificare parte dell'acqua in ghiaccio: e ciò è possibile solo se noi abbassiamo la T, da che avevamo aumentato la P => inversa proporzionalità tra P e T per l'acqua.
Mentre per la CO2, xké si ha una diretta proporzionalità tra P e T a livello della retta delle fusioni? xké per la CO2, nonké x la maggior parte delle sostanze, il volume specifico allo stato liquido è > del volume specifico allo stato solido (insomma è l'H2O ad essere strana!).
Diagramma di stato della CO2:

Facciamo un esempio:
supponiamo di avere un sistema in equilibrio tra CO2 solida e liquida, cioè stiamo su un punto della retta delle fusioni a una data T e P;
se a un certo punto noi aumentiamo la Pressione, ovvero diminuiamo il volume a disposizione del sistema, il sistema, per il Principio dell'equilibrio mobile di Le Chatelier, per non risentire dell'alterazione apportata, starà il più possibile allo stato solido dato che in tale fase “occupa meno spazio”, fondendo il più tardi possibile, cioè fondendo a una T > , da che avevamo aumentato la P => diretta proporzionalità tra P e T per la CO2!
Inoltre, notare ( facile, questo!), che per la CO2 la P atmosferica (1 atm), è ben al di sotto del punto triplo => a P atmosferica la CO2 solida (“ghiaccio secco” ) sublima, mentre il ghiaccio (dell'acqua) fonde!

Nessun commento:
Posta un commento